TRÁJER ATTILA
A Zika-jövő
A megbetegedés szúnyogvektorainak várható
elterjedése
A
Zika-járvánnyal kapcsolatos főbb ismereteket körüljáró cikkemben, ami a
folyóirat ez év márciusi számában jelent meg, bemutattam a Zika-vírus okozta
betegség felfedezésének történetét, a korábbi járványok néhány
jellegzetességét, valamint a kórokozó útját Afrikából Délkelet-Ázsiába, majd
onnan Dél-Amerikába. Írásomban ismertettem néhány fontosabb szúnyogvektor
elterjedését, valamint a betegség kórtani jellemzőit.
A
2015-ben Brazíliában kitört Zika-járvány „meghódította” Közép- és Dél-Amerikát,
és eljutott az Egyesült Államokig, ahol jelenleg behurcolt esetek formájában
van jelen. 2016. június 22-ig az Egyesült Államokban már 820 behurcolt Zika-láz
esetet regisztráltak. Az amerikai Szamoa, Puerto Rico és az Amerikai
Virgin-szigetek népessége körében viszont 1854 helyben szerzett esetet
észleltek, amiből mindössze 6 volt csak behurcolt. Elmondható, hogy jelenleg
Amerika államainak túlnyomó többségét súlyosan érinti a Zika-járvány (1. ábra).
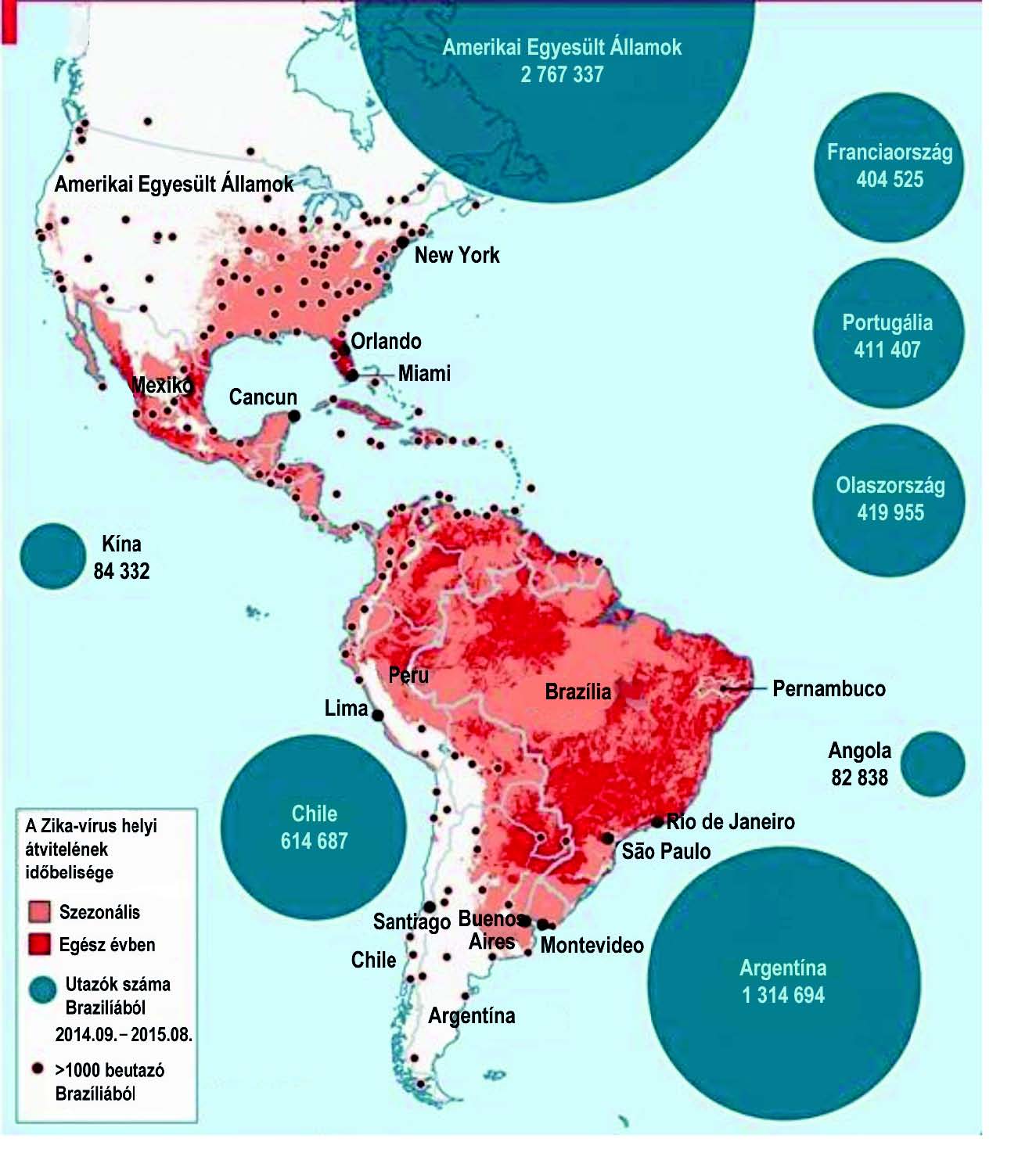
1. ábra. A Zika-láz előfordulása 2016. januárjában
Tudományos
és gyakorlati szempontból is fontos előrelépés, hogy igazolták a Zika-vírus
etiológiai szerepét a kóros kisfejűség (neonatális microcephalia)
előidézésében. Cordeiro és munkatársai (2016) 30 kisfejűséggel született
csecsemő agyfolyadékából mutatták ki a Zika-vírus ellen termelt IgM
ellenanyagok jelenlétét. 2016. május 13-ig Zika-fertőzéshez kapcsolható
veleszületett rendellenességeket nyolc országból, illetve tengeren túli
területről jelentettek: Brazília, Zöld-foki szigetek, Kolumbia, Francia
Polinézia, Martinique, Marshall-szigetek, Panama és Puerto Rico. A járvány
által érintett területen élőkön kívül négy nő: egy szlovén, egy spanyol és két
amerikai állampolgár újszülöttei esetében észleltek veleszületett
elváltozásokat. A szlovén és az egyik amerikai nő hosszabb ideig tartózkodott
Brazíliában, a másik amerikai állampolgár és a spanyol hölgy utazásuk során
fertőződtek meg a Zika-vírussal.
Az
Európai Betegségmegelőzési és Járványvédelmi Központ (European Centre for
Disease Prevention and Control, ECDC) megalkotta a Zika-fertőzés
megállapításának kritériumait, amit érdemes részletesebben is megismerni, mivel
számos elem a nem szakemberek számára is fogódzót nyújthat a diagnosztika
tekintetében.
Klinikai
kritériumnak számít, ha a betegen kiütések láthatók, ami lázzal vagy láz nélkül
jár, továbbá legalább egyet a következő tünetek közül észlelni lehet: ízületi
fájdalom, izomfájdalom vagy nem gennyes kötőhártya-gyulladás, a szemfehérje
vérbősége.
Laboratóriumi
kritériumok szempontjából a tesztek két csoportra bonthatók, az esetet
valószínűsítő és megerősítő immunológiai tesztekre. Valószínűsíthető esetről
beszélünk, ha Zika-specifikus IgM antitestek vannak a szérumban, és
megerősített esetről, ha pl. a Zika-vírusra specifikus nukleinsav mutatható ki
a mintában, vagy ha maga a vírus azonítható a mintából, de további lehetőségek
is léteznek.
Népegészségügyi
kritériumok által valószínűsíthető esetről van szó, ha az érintett személy
olyan férfival létesített szexuális kontaktust, aki a kontaktust
megelőző 3 hónapban olyan területen járt, melyet az adott időszakban
a Zika-vírus cirkuláció által érintettnek minősítettek.Amint az a leírtakból
világosan látható, megerősített Zika-esetről akkor beszélhetünk, ha a megbetegedés
tényét laboratóriumi teszttel, tesztekkel sikerült igazolni. Sem a klinikai,
sem az epidemiológiai kritériumok nem tekinthetők bizonyító erejűeknek.
A két,
világszerte elterjedt potenciális vektor Aedes faj (Aedes aegypti és Aedes
albopictus) jelen elterjedési területe együttesen lefedi az Egyesült Államok
szinte teljes keleti felét. Elmondható, hogy mindkét szúnyogfaj előfordul az
USA délkeleti államaiban, ugyanakkor az Ae. albopictus, a tigrisszúnyog
jelenlegi elterjedése jóval nagyobb, beleértve a mérsékelt övi területeket is.
Európában a helyzet magyar szemszögből ennél kedvezőbb egyelőre, köszönhetően
annak, hogy a tigrisszúnyog központi elterjedési területe főleg a
Földközi-tenger medencéjére korlátozódik, bár a faj jelenleg is terjedőben van az
öreg kontinensen. Szórványos tigrisszúnyog-előfordulásokat Csehországból,
Szlovákiából és Magyarországról is jelentettek már. A potenciális vektorok –
ahogyan arról már a márciusban megjelent cikkben is írtam – eredetileg trópusi,
szubtrópusi területek szúnyogfajai voltak. Az Ae. aegypti részéről Európát
jelenleg nem fenyegeti veszély, mivel a XXI. század utolsó évtizedeire
modellezett potenciális előfordulásának növekedése inkább a szubtrópusi
területeket veszélyezteti közvetlenül (2. ábra).
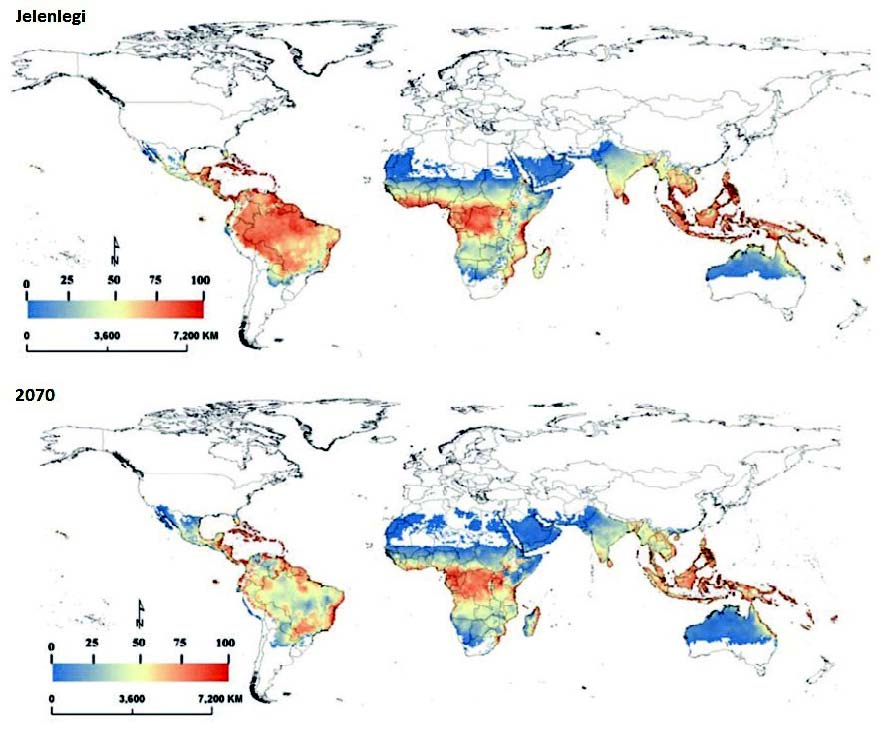
2.
ábra. Az Ae. aegypti modellezett jelenlegi (fent) és jövőbeli (lent; 2070)
elterjedési területe a SRES A1B előrejelzés szerint. A kék-vörös skála emelkedő
mértékű éghajlati alkalmassági-értéket jelenít meg (Khormi és Kumar, 2014); SRES:
Special Report on Emission Scenarios, az Éghajlat-változási Kormányközi
Testület [IPCC] által készített éghajlati előrejelzések rövidítése)
Az Ae. albopictus szúnyogfajnak mindössze az e század derekára (2045–2054) klimatikus alapon modellezett potenciális előfordulása Európában már nem ad ennyi okot a bizakodásra. Tekintve, hogy az ázsiai tigrisszúnyog jelenleg is terjeszkedik a kontinensen, várható, hogy a faj önfenntartó populációkat hoz majd létre a Kárpát-medencében a közeljövőben. Ha ez bekövetkezik, nemcsak a Zika-láz, hanem a Chikungunya- és a Dengue-láz is megjelenhet Magyarországon. Ha a nagyobb tavaink mentén található vizes élőhelyeket is kolonizálja a szúnyog, az jelentős bevételkiesést okozhat a vízparti idegenforgalomnak, nem beszélve a helyi lakosság veszélyeztetettségéről (3. ábra).

3.ábra:
Az ázsiai tigrisszúnyog (Aedes albopictus) várható elterjedése Európában a
2045–2050-es években. A sárga-vörös skála emelkedő mértékű éghajlati
alkalmassági-értéket jelenít meg (Proestos és munkatársai, 2015)
Mindenképpen szükség lenne Európában és Magyarországon is a szúnyogok aktív és rendszeres monitorozására. Egy működő megfigyelőrendszer nem képzelhető el az állategészségügy, a népegészségügy és az egyetemi kutatóhelyek összefogása nélkül. Fontos lenne, hogy a vizes élőhelyek vizsgálatában járatos egyetemi kutatóhelyek is lehetőséget kapjanak az elméleti alapok lefektetésére.
Irodalom
CDC
Stacks; Zika virus disease in the United States (06 June 2016):
https://www.cdc.gov/zika/geo/united-states.html
Cordeiro,
M. T., Pena, L. J., Brito, C. A., Gil, L. H., & Marques, E. T. (2016).
Positive IgM for Zika virus in the cerebrospinal fluid of 30 neonates with
microcephaly in Brazil. The Lancet, 387(10030), 1811-1812.
ECDC
proposed case definition for surveillance of Zika virus infection: https://ecdc.europa.eu/en/healthtopics/zika_virus_infection/patient-case-
management/Pages/case-definition.aspx
Khormi,
H. M., & Kumar, L. (2014). Climate change and the potential global
distribution of Aedes aegypti: spatial modelling using GIS and
CLIMEX.Geospatial health, 8(2), 405-415.
Proestos,
Y., Christophides, G. K., Ergüler, K., Tanarhte, M., Waldock, J., &
Lelieveld, J. (2015). Present and future projections of habitat suitability of
the Asian tiger mosquito, a vector of viral pathogens, from global climate
simulation.Philosophical Transactions of the Royal Society of London B: Biological
Sciences, 370(1665), 20130554.
Public
Health Emergency of International Concern (PHEIC) declared for Zika and
clusters of microcephaly and neurological disorders: https://ecdc.europa.eu/en/activities/sciadvice/_layouts/forms/Review
_DispForm.aspx?List=a3216f4c-f040-4f51-9f77-a96046dbfd72&ID=791
Rapid
Risk Assesment. Zika virus disease epidemic (Sixth Update, 20 May 2016):
https://ecdc.europa.eu/en/publications/Publications/
zika%20virus%20rapid%20risk%20assessment%2010-05-2016.pdf
| Természet Világa, | 147. évfolyam, 8. szám,
2016. augusztus
http//www.termvil.hu/ |