Hollósy Ferenc
A felejtés betegsége
Az
Alzheimer-kór
Meglepő,
hogy a demens betegek 58%-a jelenleg az
alacsony jövedelemmel rendelkező, sokszor élelmiszerhiánnyal küzdő országokban
él. Így elsősorban Kína, India, a
délkelet-ázsiai térség, valamint a nyugat-pacifikus térség gyorsan idősödő
lakossága érintett a kérdésben. Ez az érték 2050-re elérheti a 68%-ot. De nem
lélegezhetnek fel sem a jól szituált Amerika sem Európa országainak idősödő
korosztályai, mert őket éppúgy fenyegeti a szellemi leépülés kérdése.
Magyarországon ma körülbelül 200–300 ezer demens ember él.
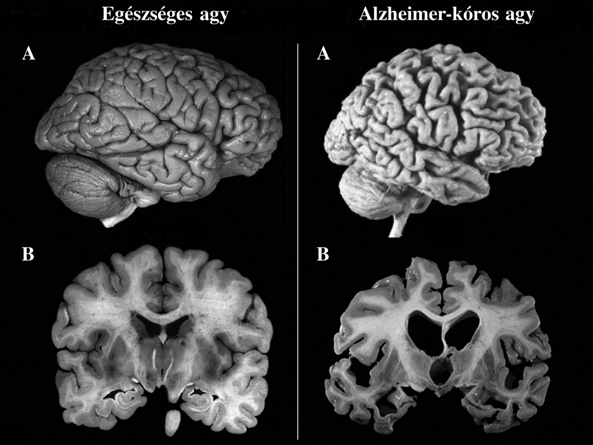
1.
ábra. Egészséges és súlyosan zsugorodott Alzheimer-kóros emberi agy
hosszmetszetben (A) és keresztmetszetben (B)
(Forrás: https://dxline.info/img/new_dictionary/alzheimers-disease_1.jpg)
A
demenciák mintegy 10%-a a visszafordítható (reverzibilis) típusok közé
tartozik, ahol a kiváltó ok kezelésével a tünetek megszüntethetők vagy
legalábbis jelentősen javíthatók. A demenciák mintegy 20%-át az ér eredetű
(vaszkuláris) demenciák közé soroljuk, melyekben a tünetek az agyi vérellátás
valamilyen zavara (érelzáródás, súlyos érszűkület) miatt alakulnak ki.
Cikkünkben a demenciák döntő hányadát, 70%-át kitevő Alzheimer-kórral
foglalkozunk. Azt a kérdéskört járjuk körül a teljesség igénye nélkül, hogy hol
tartunk jelenleg az Alzheimer-kór megismerésében és az ellene való küzdelemben?
Milyen molekuláris célpontok jöhetnek szóba a gyógyszertervezés szempontjából,
amelyekkel lassítható, vagy akár meg is állítható a betegség kifejlődése?
Tekintettel arra, hogy az Alzheimer-kór egyre több embert érint és kezelésük
egyre nagyobb financiális problémát jelent világszerte, számos kutatási és
gyógyszervizsgálati program indult a betegség okainak feltárására és
kezelésére.
Ennek
fényében meglepőnek tűnhet, hogy az intenzív kutatás ellenére több mint egy
évtizede nem került forgalomba új Alzheimer-kór elleni gyógyszer! Hogyan
lehetséges ez? Az egyik ok valószínűleg az, ami az új szerek klinikai
kipróbálása során előfordul, hogy a kutatás korai szakaszában hatékonynak és
ígéretesnek mutatkozó készítmény később a nagyléptékű klinikai vizsgálatok
során valamiért elbukik. A másik ok viszont eléggé különös. Nevezetesen az,
hogy az Alzheimer-kór pontos kiváltó okát még ma sem ismerjük!
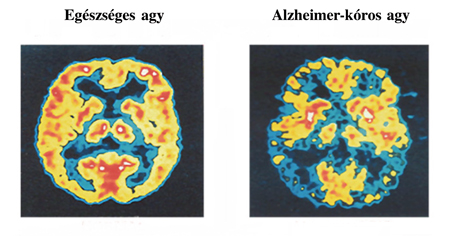
2. ábra. PET-CT felvétel az egészséges és az
Alzheimer-kóros agyról. A kék és fekete területek nagysága a betegség miatt
kieső agyi területeket jelzik (Forrás: https://healamed.com/images/stories/statia/disease/ alzheimers/alzheimers-brain-scan.jpg)
Számos tényezőről tudjuk, hogy szerepe van az Alzheimer-kór kialakulásában. Az örökletes tényezők, a magas vérnyomás, a cukorbetegség és a depresszió fontos faktorok, de vannak adatok immunológiai eltérés és anyagcserezavar alapján kifejlődött esetekre is szép számmal. Sőt! Még bizonyos étkezési szokások is gyanúba kerültek azáltal, hogy egyes betegek még kielégítő kalóriabevitel ellenére is jelentős mértékben lefogytak. Ezek után már talán nem is meglepő, hogy bizonyos szocio-ökonómiai tényezőkről is kiderült, hogy befolyással lehetnek a kór kialakulására. Az iskolázottabbaknál, a jobb jövedelmi helyzetben lévőknél és a „jobban tápláltaknál” ritkább a betegség, szemben az éhező vagy élelmiszerhiánnyal küzdő országok szegényeivel, akik között jóval gyakoribb a betegség.
Amint arról az előzőekben már szó volt, a betegség kifejlődésében az örökletes tényezők nagy szerepet játszanak. Számos génváltozatról kimutatták, hogy fokozhatja a betegség kialakulásának valószínűségét. Ilyenek bizonyos fehérjék (amiloid prekurzor fehérje, presenilin-1 és -2 fehérje, tau-fehérje) mutációi, de egyes fehérjék (apo-E fehérje) génje több változatban is előfordulhat a szervezetben (polimorfizmus). Így például az Apolipoprotein E-epszilon 4 génnek 3 különböző változatát is ismerjük, melyek csak 1–1 nukleotidban különböznek egymástól. Az eddigi vizsgálatok szerint az Alzheimer-kóros esetek 15–20%-áért ez utóbbi jelenléte a felelős, ami 17-szeresére növeli a betegség előfordulásának gyakoriságát. Ez a fehérje főleg a lipidek transzportjáért és anyagcseréjéért felelős, s mint ilyen, nem véletlenül vált intenzív vizsgálat tárgyává.
A kiterjedt kutatómunka ellenére sem tisztázott még az Alzheimer-kór pontos genetikai háttere. Pedig fontos lenne tudni, mert ma úgy gondolják, hogy az eddig megismert genetikai faktorok együtt az Alzheimer típusú demenciák akár 20–25%-áért is felelősek lehetnek.
A neuro-degeneratív betegséghez hasonlóan, Alzheimer-kór esetén is intenzív és nagyfokú neuronpusztulás figyelhető meg az agyban. A betegség jellegzetessége a fehérje-anyagcsere zavara: egy vagy több kóros konformációjú, aggregációra és plakk-képződésre hajlamos fehérjeforma alakul ki, melyek sejten belüli vagy sejtek közötti fehérjezárványok formájában halmozódnak fel. E szöveti kép miatt a neurodegeneratív betegségeket egyre gyakrabban fehérje-konformációs betegségnek tartják, vagy újabban az ubiquitin lebontási rendellenességek gyűjtőnévvel illetik, melyek patogenézisében mind a molekuláris chaperonok, mind az ubiquitin-proteaszóma rendszer fontos szerepet játszhatnak.
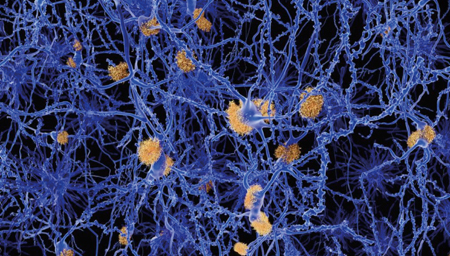
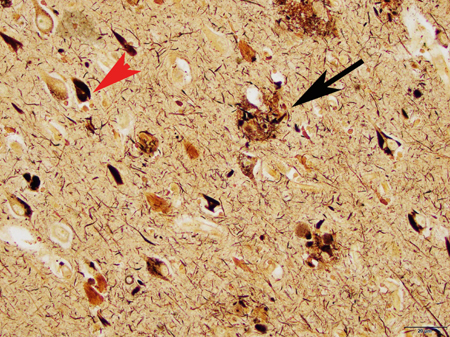
3. ábra. β-amiloid
plakkok az idegsejtek között (Forrás:
https://www.gereports.com/ brain-changes-signal-alzheimers-20-years-before-symptoms-appear/)
A
mikroszkópba tekintve az látható, hogy a betegség előrehaladásával a plakkok
változnak. A kezdetben szétszórt plakkok több lépésben érett plakkokká
alakulnak, közepén „keményítőszerűen” festődő maggal (amylum = keményítő; innen
jön az amiloid név). A mag kissé szivacsos állományú és főleg β-amiloid
peptideket, tau-fehérjét, lipofuszcint és más anyagokat tartalmaz. Az
esetek többségében csak valószínűsíthető a kórkép fennállása a beteg és a
családtagok beszámolói, a különböző gondolkodási és megismerési funkciókat
vizsgáló tesztek, a képalkotó- és
laborvizsgálatok alapján. Biztos diagnózist csak az agy szövettani vizsgálata
ad.
Az
egyes idegrendszeri degeneratív betegségeket sokszor nem könnyű egymástól
elkülöníteni, mert ugyanaz a fehérje-aggregátum többféle betegségtípusban is
megjelenhet. Alzheimer-kórban azonban jellemző az idegsejtek típusa, valamint
károsodásuk és pusztulásuk lokalizációja. A kórképek közös mechanizmusára utal
az a tény, hogy az aggregátumokat alkotó fehérjék valamennyi esetben
konformáció-változást szenvednek és fehérjekötegekké, fibrillumokká állnak
össze.
Sikerült
kifejleszteni olyan monoklonális antitesteket, melyek képesek csökkenteni a
β-amiloid szintjét az agyban, megakadályozva ezzel a plakkok kialakulását. A kór lefolyását – úgy tűnik – klasszikus
immunválasszal sikerült lassítani.
Az immunvédekezésben fontos
szerepet játszó mikrogliákat is segítségül lehet hívni az Alzheimer-kór
kezelésénél, mert szinte azonnal bekapcsolnak, amint a β-amiloid peptidek
megjelenését érzékelik. Sőt aktivitásuk annyira fokozott lehet a plakkok
jelenlétében, hogy a bontás eredményeként keletkező vegyületek már toxikusak
lehetnek a szomszédos sejtekre.
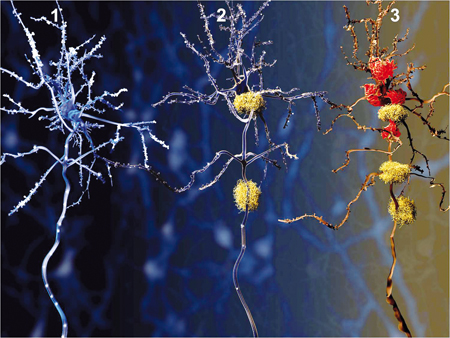
4. ábra. A három idegsejt az
Alzheimer-kóros leépülést szemlélteti. (1) egészséges neuron; (2) az amiloid plakkok sárga pamacsokként jelennek
meg az idegsejtek nyúlványain; (3) az elpusztult idegsejtet mikrogliasejtek
(piros pom-pomok) takarítják el (Forrás:
https://www.gereports.com/
brain-changes-signal-alzheimers-20-years-before-symptoms-appear/)
A β-amiloid
peptidláncához különböző típusú vegyületek kapcsolódhatnak ionos vagy
másodlagos kötésekkel. Az ilyen vegyületek megakadályozhatják a peptidláncok
aggregációját és elvileg alkalmasak lehetnek az Alzheimer-kór kezelésére.
Ezeket az anyagokat összefoglaló néven β-szerkezetrombolóknak nevezzük,
közöttük több azofesték is előfordul, ilyen például a Kongóvörös. Alzheimer
elleni hatásaikat intenzíven kutatják.
A
sejtmembrán lipidösszetétele nagymértékben befolyásolja a β- és γ-szekretáz nevű enzimek aktivitását.
Nagy mennyiségű koleszterin jelenléte a membránban növeli
mindkét szekretáz aktivitását, így a koleszterin bioszintézisét gátló
gyógyszerek jó hatással lehetnek Alzheimer-kórban. Ugyanakkor a többszörösen
telítetlen omega-3 zsírsavak jelenléte a membránban csökkentik a β-
és γ-szekretáz aktivitást és a keletkező β-amiloidok mennyiségét.
Fokozott kutatómunka folyik olyan diéta kidolgozására, amely többszörösen
telítetlen zsírsavak bevitelével akadályozza meg az Alzheimer-kór kialakulását,
illetve lassítja a betegség előrehaladását.
A tau fehérje sejten
belüli felhalmozódása miatt a kórképet ún. taupátiának is tartják. A tau
fehérje normálisan a sejtek mikrotubulus rendszerének része. Az idegsejtek
axonális transzportjában játszik fontos szerepet, mivel a sejtek ezek mentén
szállítják a különböző anyagokat az idegsejt nyúlványától (axon) a
sejttesthez, illetve onnan vissza.
A tau fehérjének 6
térszerkezeti típusa, úgynevezett izoformája ismert. Alzheimer-kórban mind a 6
izoforma kóros módosulása bekövetkezik.
A kórosan foszforilálódott (hiperfoszforiláció) tau izoformák a
sejteken belül kötegeket (aggregátumok) képeznek, melyek károsítják a
mikrotubuláris rendszert. Ezzel tönkreteszik az axonális anyagtranszportot,
mely demenciához, végül a sejtek pusztulásához vezet (pl. fronto-temporális
demencia, Pick-kór stb.).
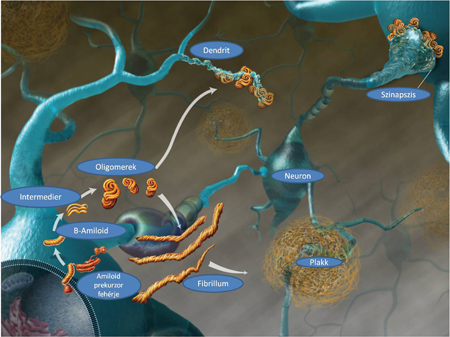
5. ábra. Az amiloid plakkok és kötegek kialakulásának fő mozzanatai (Forrás: https://theadplan.com/alzheimersdietblog/wp-content/uploads/2013/04/
Amyloid-plaque-prevention-from-fish-oil-to-help-with-Alzheimers.jpg alapján módosítva)
Fiatalabb
korban, a 40–65. életév között jelentkező Alzheimer-kórt főleg az amiloid
prekurzor protein és a presenilinek (PS1 és PS2) génjeinek
megváltozása (mutációk) idézi elő. Az amiloid prekurzor protein
normálisan egy, az idegsejtek membránjában helyet
foglaló sejtek összetapadásáért felelős fehérje (adhéziós transzmembrán
fehérje), mely fontos szerepet játszik a neuronok normális működésében, szinapszisok kialakításában.
Pontos biológiai szerepét azonban nem ismerjük.
A presenilinek számos folyamatban vesznek részt (a neuronok Ca2+ jelátvitelben, a
notch fehérje jeltovábbítási útvonalában stb.) A presenilin2
fehérje más enzimekkel együttműködve az amiloid prekurzor protein kisebb
darabokra történő hasítását végzi, minek hatására a prekurzorból nagy
mennyiségű, igen könnyen összecsapzódó, aggregálódó, az idegesejtek pusztulását
előidéző, neurotoxikus peptid képződik. A központi idegrendszert ért traumák
hatására az amiloid prekurzor protein nagy mennyiségben szabadul fel. Állandóan
ismétlődő agyi traumák, illetve oxigénhiányos állapot hatására sok amiloid
prekurzor protein termelődik, ami a már ismertetett módon β-amiloid-képződést
okoz. Ezzel magyarázzák a gyakran hipoxiás állapotba kerülő sportolók
(hegymászók, illetve búvárok), valamint a bokszolók korai demenciáját.
Az
idősebb korban kezdődő, jellemzően a 65. életév után jelentkező Alzheimer-kór
legnagyobb részénél nem ismerjük a kiváló okokat. A betegség kialakulását több
tényező is befolyásolja. Így a neurotoxikus β-amiloidok szintéziséért,
illetve lebontásáért felelős proteázok egyensúlyának zavara, az idegsejtekben
folyó ATP-termelés csökkenése (mitokondriumok sérülése), a szabad gyökök
megkötéséért felelős enzimek csökkent működése. A hazai előfordulás
tekintetében az Alzheimer-kór gyakran társul ér eredetű demenciával, amelyben
az agyi erek szűkülése, elmeszesedése (szklerózis) és a vér–agy-gát permeabilitásának
növekedése is kimutatható.
Alzheimer-kórban
az említett folyamatok eredményeként a szinapszisok sérülése és az acetil-kolin
típusú idegingerület-átvitelét végző neuronok (kolinerg neuronok) jelentős
pusztulása következik be. Az elhalt neuronokat már nem lehet pótolni, de a
patomechanizmus ismeretében ma már nem reménytelen a neuronok tömeges
pusztulása miatt bekövetkező acetilkolinszint-csökkenést
kolinészteráz-gátlókkal kivédeni. Ez természetesen csak tüneti kezelést jelent.
Újabb terápiás lehetőség a dimetil-amantadin alkalmazása. Ez ugyanis
bekötődik az N-metil-D-aszpartát-receptor (NMDA) ioncsatornájába és
megakadályozza a Ca2+-beáramlást. Ha az idegsejteket még csak
„fojtogatja” az amiloid aggregátum, és nem haltak el, a Ca2+-beáramlás
megakadályozásával ezek a sejtek „újraéleszthetők”, visszanyerik
működőképességüket.
Az idegsejtek egy
részének felszínén található ún. 5HT6 receptorokról kiderült, hogy befolyással
vannak bizonyos idegingerület átvivő anyagokra. A neurotranszmitterek mennyiségének
csökkenése kihat az idegsejtek közötti kommunikációra. Az Alzheimer-kórban
szenvedő betegek acetilkolin-szintje alacsony. Az 5HT6 receptorok gátlása
nyomán növelni lehet az acetilkolin mennyiségét, mely segíthet fenntartani az
idegsejtek normális kommunikációját.
A szakirodalom
részletesen beszámol a reaktív szabad gyököket „eltakarító” anyagok (C-vitamin,
E-vitamin, Coenzim-Q, flavonoidok) kedvező hatásáról is. Vannak növényi eredetű
szerek is, mint a Ginkgo biloba kivonatai, amelyek egyes megfigyelések
szerint lassítják az Alzheimer-kór lefolyását. Egy 2008-ban publikált nagy
amerikai vizsgálat eredménye azonban ezt a feltevést nem igazolta. Ezzel
szemben a teljesítményfokozó-készítmények (nootropikumok) családjába tartozó
gyógyszerek igazoltan javítják az idegsejtek anyagcseréjét, ennek köszönhetően
javítják a memóriát és a fókuszálási képességet. A szteroidhormonok
Alzheimer-kórra gyakorolt hatását is intenzíven kutatják.
Természetesen a
betegség gyógyszerekkel történő kémiai befolyásolásán kívül léteznek más,
fizikai és biológiai alapokon nyugvó technikák is, melyek alkalmazhatóságát
több kutatócsoport is tanulmányozza. Így például angol kutatók egy infravörös
fényt kibocsátó sisakot fejlesztettek ki, melyet a beteg fejére téve célzottan
tudják bizonyos agyterületek idegsejtjeinek működését serkenteni, elindítva
ezzel az agyterület természetes regenerációs folyamatait.
Más kutatócsoportok
nem a fényt, hanem a hangot, pontosabban az ultrahangot hívták segítségül vizsgálataikban.
A Queenslandi Egyetem kutatói gyorsan rezgő ultrahanghullámokkal aktiválták az
agy immunrendszerének részét képező mikrogliasejteket. A kutatók olyan egereket
kezeltek heteken át, amelyekben előzetesen előidézett genetikai változások
hatására agyukban jelentős mennyiségű β-amiloid rakódott le. Ultrahangos
kezeléssel 75%-uknál csaknem teljesen eltüntek a plakkok anélkül, hogy
agyszövetük látható sérülést szenvedett volna.
Őssejtek alkalmazása is szóba került az Alzheimer-kór gyógyítására. Ennek során idegi (neurális) őssejteket és
vérképzésért felelős (hemopoetikus) őssejteket együttesen ültettek be a
betegbe, és a beavatkozást bizonyos
idő eltelte után megismételték. Ezt követően a beteg kiegészítő gyógyszeres
terápiát kapott, valamint egy speciális vitaminterápiát és étrendkúrát kellett
folytatnia. Az eddigi eredmények azt
mutatták, hogy az őssejtkezelés akkor a leghatékonyabb, ha azt az Alzheimer-kór
korai stádiumában alkalmazzák. Ma az őssejtterápia egyáltalán nem
tekinthető rutineljárásnak! Sőt!
Annyira sok szereplős a beavatkozás, hogy még sikeres kezelés esetén is nyitott a kérdés: végül is melyik
lépés, sejttípus vagy molekula felelős a hatásért?
Mint
láttuk, az Alzheimer-kór ellen többfrontos harc
zajlik abban a reményben, hogy közelebb kerüljünk a betegség valódi
okainak megértéséhez. Minden sikeres vizsgálat egy-egy megnyert csatát jelent
ebben a küzdelemben. Egyre gyarapodó ismereteink és a széleskörű összefogás
adja a reményt arra, hogyha nem is tudjuk a betegséget teljesen meggyógyítani a
közeljövőben, de legalább le tudjuk annyira lassítani a szellemi hanyatlást, hogy az idős kor ne legyen egyben „idős
kór” is.
Irodalom
Penke Botond:
Neurodegeneratív betegségek kémiai és biokémiai háttere. https://chemonet.hu/osztaly/kemia/penke.html
What We Know Today
About Alzheimer’s Disease
https://www.alz.org/research/science/alzheimers_brain_tour.asp
Treatment Horizon
https://www.alz.org/research/science/alzheimers_treatment_horizon.asp
| Természet Világa, | 148. évfolyam, 3. szám,
2017. március http//www.termvil.hu/ |