IMMUNOLÓGIA
GERGELY JÁNOS
A védekezés fortélyai
Hogyan szabályozza a
sejtek és a receptorok beszélgetése
az immunfolyamatokat?
Második rész folytatás
Második rész/1
ITIM-hordozó receptorok családja
A gátló-funkciót betöltõ ITIM megismerését
követõen hamarosan kiderült, hogy az FcgRIIb
nincs monopol helyzetben, ugyanis hasonló motívumot tartalmazó
receptorok egész sora vált ismertté, továbbá
az is, hogy ilyenek nemcsak az immunrendszer sejtjein, hanem más
sejtféleségeken is megtalálhatók. Egy további
figyelemre méltó törvényszerûségre
is fény derült, nevezetesen arra, hogy az ITIM-tartalmú
receptorok ITAM-ot hordozó receptorok társaságában
fordulnak elõ. Az ITAMITIM aktiváló-gátló
páros tehát számos sejtféleségben tölt
be a B-sejteken leírtakhoz hasonló szabályozó
funkciót. Ezek funkcionális jelentõségét
az NK-sejtek példáján mutatjuk be az olvasóknak.
Az NK-sejtek. Az eddigiek során megismerkedtünk
a limfociták két jellegzetes (egymástól fénymikroszkóposan
nem különbözõ, de finomabb szerkezeti felépítésüket
és funkciójukat tekintve jelentõsen eltérõ)
populációjával, a T- és B-sejtekkel. A nyiroksejtek
egy harmadik csoportja az ún. természetes ölõsejtek
vagy NK-sejtek (Natural Killer). Ezek a limfociták antigénkötõ
sejtmembrán-receptorral nem rendelkeznek, de képesek az elpusztítandó
sejt felismerésére (ezért nevezik ezeket természetes
ölõsejteknek). Méretüket tekintve nagyobbak a nyugalmi
állapotban lévõ T- és B-limfocitáknál,
és eltérnek ezektõl abban is, hogy citoplazmájuk
számos szemcsét tartalmaz (nagy, granuláris limfociták).
Funkcionális sajátságuk, hogy a tumorsejteket
vagy a vírussal fertõzött sejteket képesek
e granulumok tartalmának segítségével elpusztítani.
Kérdés, hogyan ismerik fel az NK-sejtek az elpusztítandó
célsejtet?
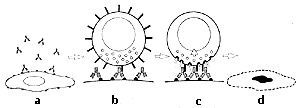 |
5. ábra. Az ADCC (ellenanyag-függô sejtközvetített
citotoxicitás) folyamata: (a) IgG molekulák kötôdnek
a sejt felszínére; (b) Az NK sejt Fcg-receptorai
köl-
csönbatásba kerülnek az IgG molekulákkal; (c) Az
Fcg-receptorok aktiválják
az NK sejteket; (d) Az akti-
vált NK sejtek elpusztítják az IgG-vel "megelölt"
sejteket. |
Az ellenanyag-függõ sejtközvetített citotoxicitás
(ADCC). Az egyik felismerési és pusztítási
mód viszonylag régóta ismert, ami az NK-sejtek membránján
megjelenõ FcgR-okkal áll összefüggésben.
Az elõbbiekben utaltunk már arra, hogy egy vírussal
fertõzött sejt vagy tumorsejt megváltozott-saját-ként
viselkedik, tehát immunválaszt indít meg. Ennek kapcsán
IgG-ellenanyagok is képzõdnek, amelyek az antigénként
viselkedõ megváltozott sejt felszínéhez kötõdnek.
Az IgG-molekulákkal borított sejt (angol kifejezéssel
target, azaz céltáblasejt) valóban céltáblaként
viselkedik, amennyiben az NK-sejtek Fcg -receptorai
a célsejtet borító IgG-molekuláknak a külsõ
környezet felé szabad Fc-részeit felismerik. Az ellenanyag
tehát fajlagosan kiválasztja, mintegy megjelöli az elpusztítandó
sejteket, majd az FcgR-okhoz kötõdve
a receptorok útján olyan jeleket vált ki az NK-sejtekben,
amelyek eredményeként azokból kiszabadulnak az addig
granulumokba zárt, sejtpusztító hatású
enzimek. Ezt a folyamatot ellenanyag-függõ, sejtközvetített
citotoxicitásnak (ADCC) nevezzük (5. ábra).
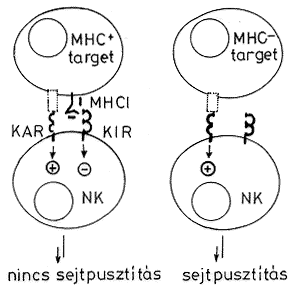 |
6. ábra. Az NK sejtek aktiválásának
és gátlásának folyamata |
NK-sejtek által közvetített, KIR-függõ
sejtpusztítás mechanizmusa. Régi megfigyelés,
hogy az NK-sejtek az elpusztítandó célsejtek között
azok MHC-I-molekulái alapján is különbséget
tudnak tenni: bizonyos NK-sejtek egy adott, míg mások egy
másik fajta MHC-I-molekulát hordozó daganatsejt vagy
vírussal fertõzött sejt elpusztítására
képesek. Ennek a szelekciónak azonban csak napjainkban derült
ki a magyarázata, nevezetesen az, hogy az NK-sejtek felszínén
található receptorok között olyanok is vannak,
amelyek a partner-sejt MHC-I-molekuláit ismerik fel. Az így
létrejövõ kölcsönhatás azonban nem
aktivációs, hanem gátló jeleket továbbít,
ezért ezeket a receptorokat ölést gátló
(killing inhibitory receptors KIR) receptoroknak nevezik (6. ábra).
A KIR szerkezetének tanulmányozása azt mutatta,
hogy az extracelluláris részen elhelyezkedõ ligandumkötõ
hely más és más MHC-I-molekula felismerésére
alkalmas, a receptor citoplazmatikus szakasza pedig ITIM-motívumot
tartalmaz. A KIR és a megfelelõ MHC-I-molekula között
kialakuló kapcsolat éppúgy, mint a BCR-Fcg
RIIb kölcsönhatás a B-sejteken foszfatázok aktiválása
és következményes defoszforilációs folyamatok
révén gátolja az egyébként sejtpusztítást
eredményezõ aktivációs jeleket.
A vírussal fertõzött sejtek (lásd késõbb)
és a daganatsejtek egyik sajátsága, hogy teljesen
vagy jelentõs mértékben megszûnik az MHC-molekulák
megjelenése e sejtek membránján. Ennek következtében
a KIR nem talál ligandumot (MHC-I-molekulát) a partnersejt
felszínén, nem tud tehát gátló jeleket
közvetíteni, és így a sejtpusztítást
eredményezõ aktivációs folyamatok érvénysülésének
akadálya nincs. Az eredmény: az NK-sejt elpusztítja
a vírussal fertõzött sejtet vagy daganatsejtet. (Az
NK-sejteken a KIR mellett, ezektõl eltérõ szerkezeti
sajátságú, de ITIM-motívumot a citoplazmatikus
részben ugyancsak tartalmazó, és hasonló funkciót
betöltõ egyéb receptorok is találhatók.
Ezek mûködési elve megegyezik a KIR-ével, ezért
ezek ismertetésére itt nem térünk ki.)
A vírusok MHC-stratégiája
A vírussal fertõzött sejtet az (immunrendszer részérõl)
az MHC-molekulákkal is összefüggõ, legalább
kétféle veszély is fenyegeti. Az egyik, hogy a vírusantigén
az MHC-I-molekulával komplexben jelenik meg a fertõzött
sejt felszínén, és a citotoxikus T-sejtek (CTL) ezt
a komplexet felismerve pusztítják el a vírussal fertõzött
sejtet, gátolva ezzel a kórokozó fennmaradását.
A másik veszélyt az jelenti, hogy ha a vírusfertõzés
következtében már csökkent a fertõzött
sejtek membránján megjelenõ MHC-molekulák száma,
azok az NK-sejtek áldozataivá válva elpusztulnak.
A vírusok számos módon védekeznek
az immunrendszer pusztító hatása ellen, egyebek között
úgy is, hogy hatásukra csökken a fertõzött
sejt felszínén az MHC-I-molekulák megjelenése
a fertõzött sejt membránján. Egy másik
része a vírus MHC-stratégiájának az,
hogy befolyásolja a fertõzött sejt antigént feldolgozó
és bemutató (prezentáló) folyamatait. Ennek
eredményeként csökken vagy teljesen eltûnik a
víruseredetû peptideket tartalmazó MHC-I-molekulák
száma a fertõzött sejt felszínén, a citotoxikus
T-limfocitáknak tehát nincs mit felismerni a vírussal
fertõzött sejtek felszínén, tehát dolgavégezetlenül
távoznak a sejt közelébõl.
Ismervén azonban az NK-sejtek által közvetített
sejtpusztítás mechanizmusát, azt hihetjük, hogy
a vírus az MHC-stratégiával öngólt lõtt,
hiszen az MHC-I-molekulák számának csökkentésével
egyúttal megszûnik a KIR közvetített gátló
folyamat, és az NK-sejtek teljesíthetik pusztító
hivatásukat. A vírusok azonban ezt a problémát
is megoldják. Ismerünk ugyanis olyan vírusokat, amelyek
a sejteket arra késztetik, hogy azok szerkezetileg az MHC I-hez
hasonló molekulákat termeljenek. A hasonlóság
olyan mértékû, hogy a KIR-receptorok azokat felismerve
gátló szignáljaikat változatlanul továbbíják
az NK-sejtek felé. Ez az ál MHC-I-molekula azonban eltérõen
az eredetitõl nem alkalmas az antigén eredetû pepidek
megkötésére. A vírus MHC-stratégiája
tehát elérte a célját: nincs antigén
prezentáció, következésképpen a CTL nem
tudja elpusztítani a vírussal fertõzött sejtet;
az NK-sejtek KIR-receptora felismeri az ál MHC-I-molekulát,
és folyamatosan gátolja a sejpusztító hatás
érvényesülését.
A nagy kérdés az, kutatásaink mikor jutnak
el arra a szintre, hogy az ITAMITIM-motívumok közvetítette
receptorok közötti beszélgetést a vírusok
és a daganatsejtek elleni küzdelem érdekében
is fel tudjuk használni.
| Természet Világa, |
129. évf. 12. sz. 1998. december, 534539. o.
https://www.kfki.hu/chemonet/TermVil/
https://www.ch.bme.hu/chemonet/TermVil/ |
Vissza a tartalomjegyzékhez

