A különböző technológiák és találmányok működése sok esetben a természettudósok által megfigyelt és leírt természeti jelenségen alapul. Talán a legközismertebb ezek közül a repülőgép, amelynek tervezéséhez Leonardo da Vinci és a Wright fivérek is a madarak repülését tanulmányozták [1]. A természetet utánzó mérnöki megoldásokra több kifejezés is létezik, amelyek többé-kevésbé rokon értelműnek tekinthetők.
A bionika szó jelentése az amerikai légierőnél dolgozó Dr. Jack E. Steele 1960-as megfogalmazása szerint biológiai minták alkalmazása mesterséges rendszerek megtervezésére. A köznyelv azonban (elsősorban a filmipar hatására) a bionikát később tévesen az elektromos vezérlésű protézisekkel azonosította, így manapság inkább a biomimetika, illetve biomimikri fogalmak használatosak a természetet ihlette mesterséges eszközök, technológiák leírására. (Ezek a görög biosz = élet és mimézis = utánzás szavakból erednek [2].) A műszaki megoldások nem feltétlenül másolatai a biológiai rendszereknek, sok esetben csupán inspirációt jelentenek a tervezők számára [3].
A természetet utánzó megoldások
A természetet utánzó találmány például a tépőzár, amelyet a ruhákra tapadó bogáncs ihletett, valamint a hajók cápabőrhöz hasonló, közegellenállást csökkentő bevonata. Az elefántok ormányának mintájára gyártott ipari anyagmozgató gépek nagy erő kifejtésére képesek, pontosságuk és flexibilitásuk révén bonyolult mozdulatok precíz kivitelezésére is alkalmasak.
Egy különleges „vízgyűjtő kulacs” alapötletét a Namib-sivatagban élő bogárfaj adta. Ez a bogár a hajnali ködben beáll a széllel szembe, így a fedőszárnyán lévő, hidrofil felületű dudorokon a nedvesség vízcseppekké áll össze, a dudorok közti hidrofób mélyedéseken keresztül pedig a cseppek lefolynak a bogár rágószervébe. Ezt utánozza az alakja után citromfacsaróra emlékeztető vizes palack (1. ábra), amely száraz, sivatagos területeken lehetővé teszi az életmentő ivóvíz gyűjtését [4].

Vízkezelés
A vízkezelés a megfelelő víztisztítási eljárások gyűjtőfogalma. Akár ivóvízről, akár ipari célra szánt vízről (például kazántápvíz, hűtővíz, ultratiszta víz stb.) legyen szó, a természetes vizeket csak megfelelő kezelés után tudjuk hasznosítani. A felhasználás során megváltozik a víz összetétele és egyéb tulajdonságai, így ismét kezelni kell ahhoz, hogy elérje a kielégítő minőséget a befogadóba (például folyóba vagy tóba) való juttatáshoz, tehát a szennyvíz-tisztítási eljárások is ide tartoznak. A végtermékként kapott tisztított víz számos paraméterének meg kell felelnie az adott határértékeknek; ezek lehetnek ipari előírások a technológiai felhasználásnál, illetve hatósági előírás az ivóvíz, vagy a befogadóba bocsátás esetén.
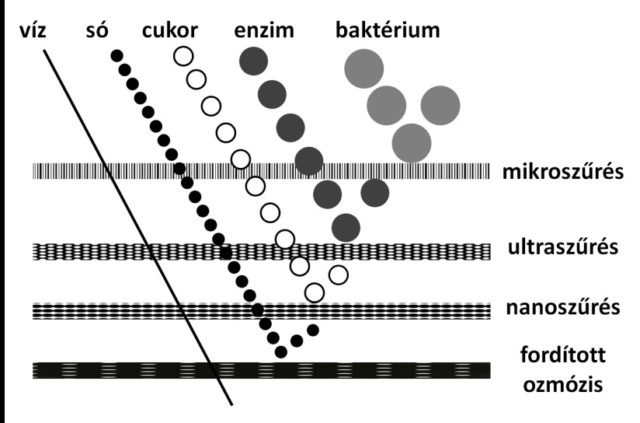
A vízkezelési technológiák igen szerteágazóak, ugyanakkor mindegyiknek része egy vagy több szűrési lépés, amelyet manapság jellemzően membránok segítségével végeznek. A szűréshez használt membránokat csoportosíthatjuk aszerint, hogy mekkora részecskéket engednek át; ezt szemlélteti a 2. ábra. Így megkülönböztethetünk mikroszűrést, ultraszűrést, nanoszűrést és fordított ozmózist.
A szűrés során a membrán egyik oldalán keringetett folyadékra (kezelendő víz) nyomást fejtenek ki, amelynek hatására a membrán pórusainál kisebb molekulák átáramlanak a másik oldalra, a nagyobb molekulák viszont nem férnek át, így a kiindulási folyadékban maradnak. Minél kisebbek ezek a pórusok, annál kisebb részecskéket tartanak vissza, illetve annál nagyobb nyomásra van szükség, hogy „átpréseljük” rajtuk a molekulákat. Így például ultraszűrésnél elegendő 1-10 bar nyomást alkalmazni, de fordított ozmózis membránnál már 20-100 bar nyomásra is szükség lehet (például tengervíz sótalanításánál).
A membrános eljárások között már említett fordított ozmózis (röviden RO az angol reverse osmosis kifejezésből) mellett létezik egy direkt ozmózis (forward osmosis, FO) nevű vízkezelési (membrános) eljárás is, amelyet szintén víz nyerésére fejlesztettek ki, s amely lehetővé teszi, hogy ivóvizet állíthassunk elő bármilyen szennyezett vízforrásból (akár egy pocsolyából) egyetlen készülék segítségével, elektromos áram, szivattyú… stb. nélkül. Ahogy a nevük is mutatja, mindkét eljárásnál kulcsfontosságú az ozmózis jelensége, ami egy hétköznapi életből vett példával könnyen szemléltethető. Képzeljünk el egy szem mazsolát, amelynek belsejében nagymennyiségű cukor található. A mazsola héja jelenti példánkban a membránt, amely a víz számára bizonyos mértékben átjárható, a cukrot viszont visszatartja. Ha ezt a mazsolát egy tál vízbe helyezzük, környezetéből vizet vesz fel és megduzzad. A természet ugyanis igyekszik kiegyenlíteni a membrán két oldala (mazsola belseje és környezete) közti koncentrációkülönbséget. A cukor azonban nagy mérete miatt nem juthat ki a mazsolából, ezért „helyette” víz áramlik be, s igyekszik hígítani a mazsola belsejében a cukor oldatot, ezt a folyamatot hívjuk ozmózisnak (3. ábra).
Ez a jelenség játszódik le a direkt ozmózis során, amikor egy híg oldat felől víz áramlik a tőle membránnal elválasztott töményebb oldat felé. Az említett FO példánál tömény cukros, vitaminos oldat található a membrán egyik oldalán, s a külső térben található víz molekulák ezt igyekeznek hígítani, átáramolnak a membránon, s iható folyadékot lehet nyerni.
A fordított ozmózis abban különbözik ettől, hogy ez esetben nem hagyjuk magára a rendszert, hanem – az ozmózist legyőzendő – nagyobb nyomást gyakorolunk a töményebb oldatra, így a töményebb oldatból áramlik tiszta víz a hígabb oldat felé. A fenti példánál maradva ez olyan, mintha a mazsolát nem hagynánk megduzzadni, hanem összenyomnánk és kipréselnénk belőle a vizet.
Az ozmotikus víztisztítási eljárások használhatók szennyezett vizek kezelésére, tengervíz sótalanítására édesvíz előállítása céljából, valamint az elektronikai iparban szükséges ultratiszta víz termelésére.
Szűrés több lépésben
Membránszűrés nemcsak az ember által alkotott vízkezelési technológiákban fordul elő. Kiválasztó szervrendszerünk működése lényegében többlépéses szűrési eljárásnak tekinthető, amelynek során a szelektív transzport a sejteket határoló kettős lipidrétegen, a sejtmembránon keresztül zajlik. Egy egészséges felnőtt emberben átlagosan napi 180 liter filtrátum (elsődleges szűrlet) keletkezik, a napi vizeletmennyiség viszont csupán 1-2 liter, tehát a szűrlet mintegy 99 százaléka visszaszívódik! Ezt a hihetetlen teljesítményt a vese bizonyos sejtjeiben található vízcsatorna fehérjék, az akvaporinok teszik lehetővé [7].
Az akvaporinok a sejtmembránba ágyazott (úgynevezett transzmembrán) fehérjék, amelyek a biológiai sejtek vízáteresztő képességét szabályozzák a vízmolekulák teljesen szelektív és megdöbbentő sebességű transzportja révén. Felfedezésük Peter Agre amerikai tudós nevéhez fűződik, aki 1991-ben igazolta a vízcsatornák létezését és leírta szerkezetüket, munkásságáért pedig 2003-ban kémiai Nobel-díjat kapott [8]. A ’90-es években együtt dolgozott a Pécsi Tudományegyetem több munkacsoportjával, ennek elismeréseként 2006-ban az egyetem Egészségügyi Főiskolai Karának díszdoktorává avatták [9]. Az együttműködés során Dóczi Tamás, az egyetem idegsebészeti klinikájának akkori tanszékvezető tanára vezetésével bebizonyították, hogy az akvaporin-4 fehérje blokkolása hatékony agyödéma-ellenes kezelés lehet [10].
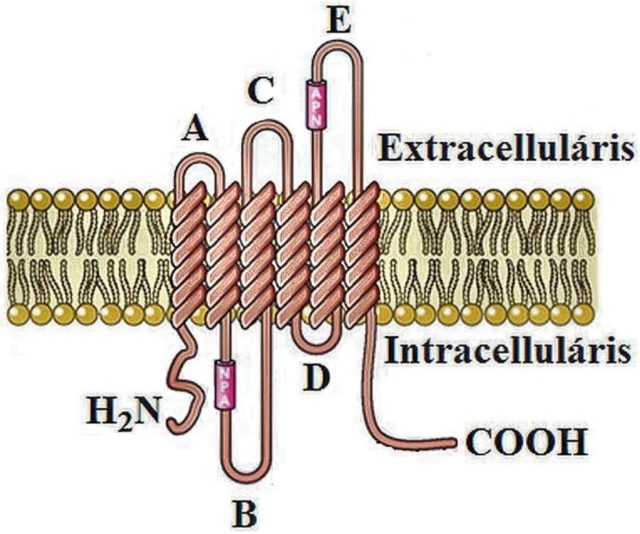
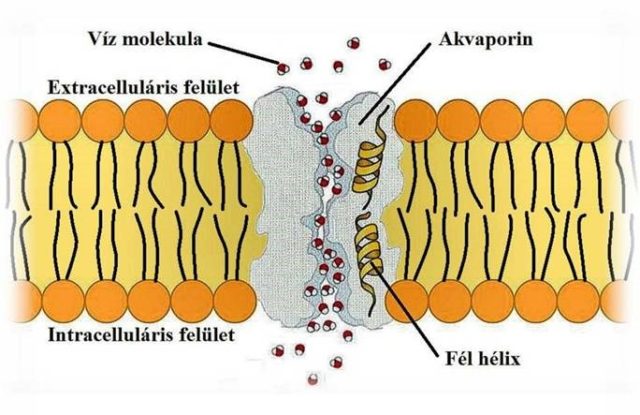
Az akvaporin fehérje hat α-hélixet tartalmaz, s a polimerlánc úgy épül be a sejtmembránba, hogy több helyen „keresztezi” azt, a protein belsejében pedig egy csatorna alakul ki (4. ábra). Ez a központi üreg a legszélesebb részén is mindössze 15 Å átmérőjű (egy angström a milliméter tíz-milliomod része!), így a víznél nagyobb molekulákat méretük alapján kizárja. A szelektivitást elősegíti továbbá a csatornában elhelyezkedő aminosav szekvencia, amelyet aromás/arginin (Ar/R) filternek neveznek. Ez a klaszter hidrofób aromás aminosavakat és arginint tartalmaz, amely parciális pozitív töltést visz a rendszerbe. Ráadásul két úgynevezett fél-hélix a fehérje szalagon belül permanens dipólust formál, s így nettó pozitív töltés alakul ki a fehérje csatorna közepén, ami elektrosztatikus gátat emel a pozitív töltésű részecskék útjába (5. ábra) [8].
Két aminosav triplet: aszparaginsav, prolin és alanin szintén megjelenik az akvaporin szekvenciában. Ezek a tripletek – amelyeket NPF motívumoknak hívnak – hidrogénkötést alakítanak ki a bejövő vízmolekulákkal. Ahogy a víz molekulák elhaladnak az NPF motívumok mellett, reorientálódnak oly módon, hogy a protonok ne ugorhassanak át a szomszédos víz molekulákra, s így a protonok áramlását teljesen megakadályozzák. Ennek a szerkezeti felépítésnek köszönhetően az akvaporinok vízáteresztő képessége a 6.10-14 – 11.10-14 cm3/s tartományban van csatornánként, ami körülbelül 3 milliárd vízmolekulát jelent másodpercenként! Mindeközben az ionok jelentős részét visszatartják [11].
Gyorsabb membránok
Mintegy egy évtizeddel az akvaporinok felfedezését követően fogalmazódott meg a gondolat, hogy a biológiai membránok utánzásával a vízkezelésben használatos FO és RO membránok szelektivitását és permeabilitását növelni lehetne [12]. A sejteket határoló membránok lényegében egy kettős lipidrétegből és a beágyazott fehérjékből épülnek fel. A hidrofil „fejből” és a hozzá kapcsolódó két hidrofób „farokból” álló lipidmolekulák a hidrofób részükkel egymás felé fordulva kétrétegű struktúrát hoznak létre, amelynek külső felülete hidrofil, a rétegek között pedig hidrofób karakterű (5. ábra). Ha egy ilyen lipidréteget membránként használnánk, és a lipid-protein arányt 50 körül állítanánk be, egy négyzetméternyi felületen 9-16 liter vizet lehetne átszűrni egy óra alatt, míg a kereskedelmi forgalomban kapható RO membránnal csupán 2-5 litert. Tehát az akvaporin membrán négyszer gyorsabb szűrést tesz lehetővé az elméleti számítások szerint [10][12].
A biomimetikus membránok gyártása azonban nem egyszerű, hiszen az akvaporinok számára természetes nyomás, hőmérsékleti és ozmotikus viszonyok, amelyek a sejtjeinkben fennállnak, nagymértékben eltérnek a vízkezelés során jellemző paraméterektől. A fehérjék pedig igen érzékenyek a környezeti körülményekre, könnyen elveszthetik aktivitásukat. Éppen ezért eleinte csak direkt ozmózis céljára készítettek akvaporin-tartalmú membránokat, mivel itt „csak” az ozmózisnyomást kell elviselni a membránnak, szemben a fordított ozmózisnál alkalmazott 20-100 bar nyomáskülönbséggel. Ugyanakkor az ozmózisnyomás értéke sem elhanyagolható, például tengervíz esetében ez körülbelül 25 bar, tehát már a direkt ozmózisnál is fontos a kellő mechanikai stabilitás biztosítása [6]. A technika fejlődésével később megjelentek az RO membránok is, eleinte csak kísérleti berendezésekben, de ma már kereskedelmi forgalomban is kaphatók [14].
A megfelelő teljesítményű membrán gyártásához nagy mennyiségű protein beágyazása szükséges oly módon, hogy természetes aktivitásukat megőrizve biztosítsák a kívánt permeabilitást és szelektivitást, ugyanakkor kellő stabilitással rendelkezzenek az üzemeltetés során fellépő nyomás elviseléséhez [11]. A legelterjedtebb megoldás erre a feladatra a proteo-liposzómák alkalmazása. Ahogy nevük is utal rá, ezek kettős lipidrétegből álló „gömbök” (vezikulumok), amelyekbe beágyazódnak az akvaporinok, így lényegében a sejtmembránhoz hasonló szerkezet jön létre [13].
A proteo-liposzómás FO és RO membránok alapvető felépítésükben megegyeznek: alapjuk egy támasztóréteg, amely a mechanikai szilárdságot biztosítja, erre kerül egy szelektív fedőréteg, amelybe beágyazva találhatók a vezikulumok (6. ábra). A pórusos támasztóréteg többnyire valamilyen polimerből, például poliszulfonból készül [15]. A stabilitás növelése érdekében ezt egyéb, nemszőtt támasztó anyaggal is kiegészíthetik [13].
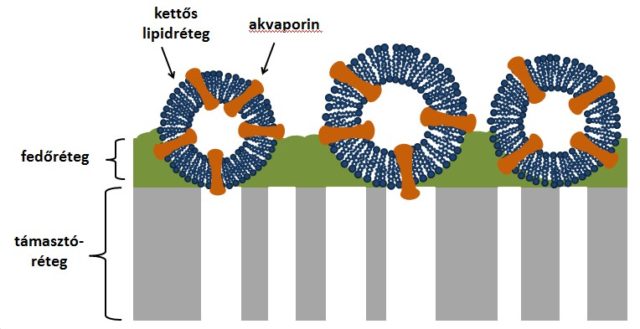
A támasztóréteget ezután fedőréteggel vonják be, amely szintén polimer anyagú. (Többnyire kompozit membránokat készítenek, ami azt jelenti, hogy a két réteg különböző anyagú.) A szelektív réteg kialakítása határfelületi polimerizációval történik. Az eljárás lényege, hogy az egyik monomer vizes oldatába merítik a pórusos támasztóréteget, majd a másik monomer vízzel nem elegyedő oldatába teszik, a két oldószer határfelületén pedig végbemegy a polimerizáció. Így egy rendkívül vékony fedőréteget kapunk, a vékonyabb membrán pedig kisebb ellenállást jelent az üzemeltetés során [6]. A proteo-liposzómát tartalmazó oldatot az egyik monomeroldathoz keverik, ennek eredményeként a polimerréteg a vezikulumok körül alakul ki. A makromolekulákat összekapcsoló, úgynevezett keresztkötő ágensek adagolásával tovább segíthető a liposzómák beágyazása [16]. Az FO és RO membránok gyártásának alapjai tehát azonosak, de az egyes rétegek anyaga, kialakítása, pórusmérete stb. nagymértékben eltérhet.
Az így kialakított akvaporin membránok – ahogyan az várható volt – nagyobb mértékben képesek átengedni a vízmolekulákat, mint a hasonló felépítésű, de akvaporint nem tartalmazó membránok. Dán kutatók méréseik alapján megállapították, hogy direkt ozmózisnál 1 m2-nyi felületű membránnal óránként 23 liter vizet tudtak kinyerni az akvaporinos membránnal, míg nélküle 16 litert [12]. Hasonlóan sikeresek a laboratóriumi kísérletekben a fordított ozmózis membránok is [14].
Mesterséges vízcsatornák
A természetes forrásból származó akvaporinok membránba ágyazása mellett felmerül a mesterséges vízcsatornák létrehozásának lehetősége is. Itt valódi értelemben vett biomimikriről van szó, hiszen a sejtfalban található fehérjéket utánzó, szintetikus csatornák kialakítása a cél, amelyek a természeteshez hasonló szelektivitást és permeabilitást biztosítanak. Az akvaporinok képesek önszerveződő módon beépülni a biológiai membránba, pontosan illeszkedő csatornákat hozva létre ezáltal, továbbá szerkezetüknek köszönhetően a vízmolekulák egyesével, sorban haladva jutnak át rajtuk, ami segíti az ionok visszatartását a korábban leírtak szerint. A szintetikus membránoknak meg kell felelniük ezeknek az elvárásoknak, ugyanakkor a fehérjéknél nagyobb mechanikai és kémiai stabilitással kell rendelkezniük.
A csatornák felépülhetnek kis méretű szerves molekulákból, amelyek hidrogénkötéssel vagy hidrofób kölcsönhatások révén kapcsolódnak egymáshoz, illetve a membrán pórusainak falához. Ilyen molekulák lehetnek például dipeptidek, amelyek a fehérjékhez hasonló víztranszport megvalósítására képesek, ugyanakkor hőstabilitásuk viszonylag gyenge.
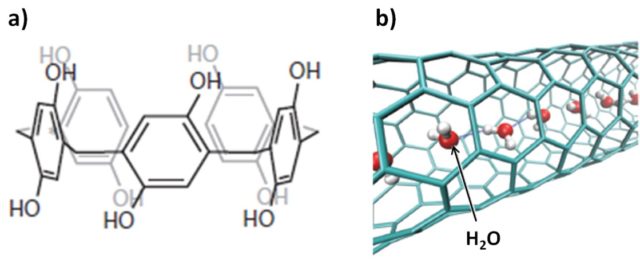
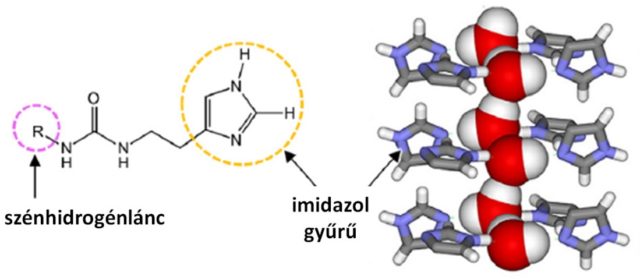
Az imidazol-kvartett csatornáknál körben négy imidazol gyűrű helyezkedik el, a hozzájuk kapcsolódó szénhidrogénláncok pedig a membránba ágyazódást teszik lehetővé (7. ábra). Hasonló struktúra kialakítására számos gyűrűs molekulát próbálnak ki a kutatók, ezek méretétől és felépítésétől függően általában négy-hat vegyület kapcsolódik össze egy síkban.
Emellett olyan szerkezettel is kísérleteznek, ahol egyetlen molekula alkot egy kört, ezek egymásra rétegződésével alakul ki a csatorna. Többen foglalkoznak a szén-nanocsövek vízcsatornaként történő alkalmazásának lehetőségével is, ezek hatékonysága azonban egyelőre vitatott (8. ábra).
Az akvaporinok szintetikus helyettesítésére tehát számos alternatíva merül fel, amelyek jellemzően még alapkutatási stádiumban vannak. A kutatóknak az áteresztőképességi, szelektivitási és stabilitási tulajdonságokon túl figyelmet kell fordítaniuk a későbbi ipari léptékű gyártás gyakorlati kihívásaira és anyagi vonzataira is [18]. Az viszont biztos, hogy a cikk elején említett példákhoz hasonlóan az akvaporinok felfedezése és leírása is nem várt gyakorlati haszonnal járt, érdemes tehát a műszaki élet kihívásainak megoldásakor időről-időre ihletet merítenünk a természetből.
BÉLAFINÉ BAKÓ KATALIN – TAKÁCS PIROSKA
KÖSZÖNETNYILVÁNÍTÁS
A kutatómunka részben az Ozmotikus hatásokon alapuló koncentrálások vizsgálata című, 2018-2.1.11-TÉT-SI-2018-00001 számú kétoldalú, szlovén-magyar együttműködési projekt támogatásával készült.
IRODALOM
[1][3] http://ofi.hu/7-evfolyam (Oktatáskutató és Fejlesztő Intézet: Bionika, biomimetika, biomimikri – összefoglaló háttéranyag)
[2] https://www.origo.hu/tudomany/20100220-e.html (Pesthy Gábor: Élőlények a mérnökök szolgálatában, 2010.)
[4] http://elteonline.hu/tudomany/2017/05/10/technologiak-amiket-a-termeszettol-csentunk/ (Tankó Andrea: Technológiák, amiket a természettől csentünk, 2017.)
[5] https://www.forwardosmosistech.com/the-principles-of-forward-osmosis/Mark Perry: The principles of forward osmosis (FO), 2013.)
[6] Bélafiné dr. Bakó Katalin: Membrános műveletek, Veszprémi Egyetemi Kiadó, Veszprém, 2002
[7] Fonyó Attila: Az orvosi élettan tankönyve, Medicina Könyvkiadó Zrt., 2011
[8] L. Simon Á.: Megtalálták a kiskaput. Nobel-díj a membráncsatornák felfedezéséért. Természet Világa 135(2) (2004) 54-56
[9] https://pte.hu/diszdoktorok/dr-peter-agre
[10] Kis színes csevej Dóczi Tamással (Braun Tibor rovata), Természet Világa 136(6) (2005) 275-
[11] Y. Kaufman and V. Freger, „Supported Biomimetic Membranes for Pressure-Driven Water Purification,” in On Biomimetics, 2011.
[12] C. Y. Tang, Y. Zhao, R. Wang, C. Hélix-Nielsen, and A. G. Fane, „Desalination by biomimetic aquaporin membranes: Review of status and prospects,” Desalination, 308, pp. 34–40, 2013.
[13] Y. Chun, L. Qing, G. Sun, M. Roil, and A. G. Fane, „Prototype aquaporin-based forward osmosis membrane: Filtration properties and fouling resistance,” Desalination, 445, pp. 75–84, 2018.
[14] https://aquaporin.com/products/
[15] Y. Li, S. Qi, M. Tian, W. Widjajanti, and R. Wang, „Fabrication of aquaporin-based biomimetic membrane for seawater desalination,” Desalination, 467, pp. 103–112, 2019.
[16] M. Xie, W. Luo, H. Guo, L. D. Nghiem, C. Y. Tang, and S. R. Gray, „Trace organic contaminant rejection by aquaporin forward osmosis membrane: Transport mechanisms and membrane stability,” Water Res., 132, pp. 90–98, 2018.
A cikk a Természet Világa 2020. augusztusi számában (151. évf. 8. sz.) jelent meg.